Bosquejo Examen Final de Semestre - Diciembre 2013
I.
Vocabulario
1)
Solución
2)
Solvente
3)
Soluto
4)
Coloide
5)
Suspensión
6)
Solución diluida
7)
Solución concentrada
8)
Solubilidad
9)
Solución saturada
10)
Solución no saturada
11)
Solución supersaturada
12)
Ácidos
13)
Bases
14)
Corrosivo
15)
Indicador
16)
Neutralización
17)
Digestión
18)
Digestión química
II.
Soluciones, coloides y suspensiones
1)
¿Cuáles son las características de las
soluciones, coloides y suspensiones?
2)
¿Qué sucede con las partículas de soluto cuando
una solución se forma?
3)
¿Cómo los solutos afectan los puntos de congelación
y los puntos de ebullición del solvente?
III.
Concentración y solubilidad
1)
¿Cómo se mide la concentración? (Ejercicios
problemas verbales)
2)
¿Cómo se utiliza la solubilidad para identificar
sustancias?
3)
¿Qué factores afectan la solubilidad en una solución?
IV.
Ácidos y Bases
1)
¿Cuáles son las propiedades de los ácidos y las
bases?
2)
¿Cuáles son los ácidos y las bases más comúnmente
usadas?
3)
¿Qué se forma cuando se mezcla un ácido con
agua?
4)
¿Qué se forma cuando se mezcla una base con
agua?
5)
Escala de pH
·
¿Qué es?
·
¿Qué te dice acerca de la solución?
6)
¿Qué sucede en una reacción de neutralización?
V.
Digestión y pH
1)
¿Cómo el pH afecta la digestión del ser humano?
Repaso Examen #4: Reacciones químicas
Vocabulario:
1.
Ecuación química
2.
Reactivos
3.
Productos
4.
Conservación de masa
5.
Sistema abierto
6.
Sistema cerrado
7.
Precipitado
8.
Reacción endotérmica
9.
Reacción exotérmica
10.
Coeficiente
11.
Energía de activación
12.
Concentración
13.
Catálisis
14.
Enzima
15.
Inhibidor
16.
Combustión
·
Evidencia de reacciones químicas.
·
Conservación de masa
o
¿Qué es conservación de masa?
o
Algunos ejemplos pagina 196 libro de texto,
ejercicio 2b “assessment” pagina 201 libro de texto.
·
Saber ofrecer ejemplos de sistema cerrado y
sistema abierto.
·
Energía de activación
o
¿Qué es energía de activación?
o
Saber explicar las gráficas de energía de activación.
o
Saber diferenciar una gráfica de reacción endotérmica
y una gráfica de reacción exotérmica
o
Resolver ejercicios de práctica 21-22 pagina 218
libro de texto.
·
Cuatro áreas que los científicos pueden
controlar durante una reacción química y saber explicar cada una de ellas.
·
Balanceo de ecuaciones químicas
o
Resolver ejercicios de practica 17-20 página 218
libro de texto
·
Clasificación de reacciones química.
o
Estudiar los 4 tipos (síntesis, descomposición, sustitución
simple y sustitución compleja)
o
Realizar los ejercicios de práctica 14 pagina
218 libro de texto.
***Repasa
los “key Concepts” 1, 2 y 3 de la página 216 libro de texto
***Repasa el
“assessment” de la página 201 libro de texto
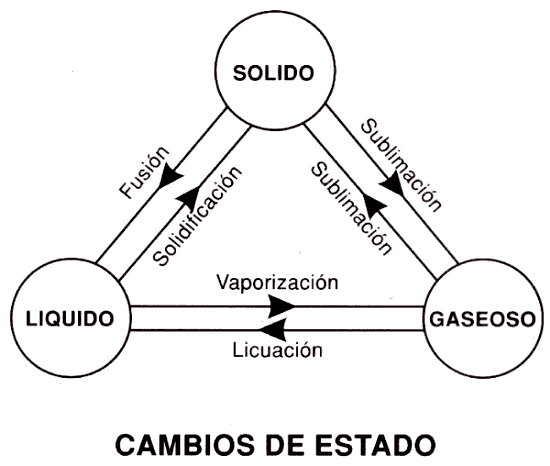
Cambios Químicos y Físicos
Fecha Examen # 1: 27 de agosto de 2013
Maestra ya que el viernes fue el pep rally y 8-3 no tuvo educacion fisica el miercoles el dia del examen yo creo que no tendremos su clase.Para contestarme :jcf0623@gmail.com 3-6pm. GRACIAS
ResponderBorrarBuenas,lo de las evidencias de las reacciones quimicas es mencionarlos solamente?
ResponderBorrar